トピックス
HTLV-1潜伏感染の鍵となる「ウイルス内サイレンサー」の発見:RUNX複合体による転写抑制機構
HTLV-1は自らのゲノムに「活動を抑え込む配列」を持ち、免疫監視を回避して長期持続感染を成立させる
ポイント
- HTLV-1プロウイルス内に、ウイルス遺伝子発現を抑制する「サイレンサー領域」を同定した。
- サイレンサーの破綻によりウイルス活性が亢進し、潜伏が解除され免疫排除されやすくなることを実証した。
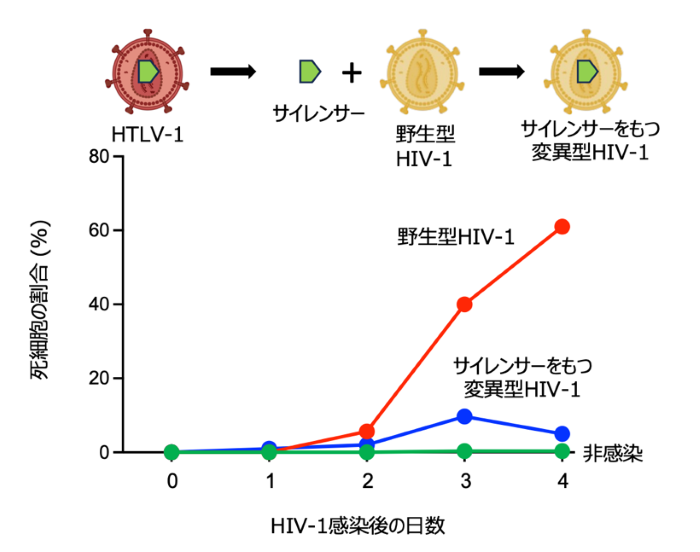
- 同領域をHIV-1へ導入すると、HIV-1のウイルス産生が抑制され「潜伏しやすい状態」へ変化することを示した。
- 宿主転写因子RUNX1を中心とする複合体がサイレンサーに結合し、HTLV-1の転写(転写バースト)を抑える機構を明らかにした。
研究背景
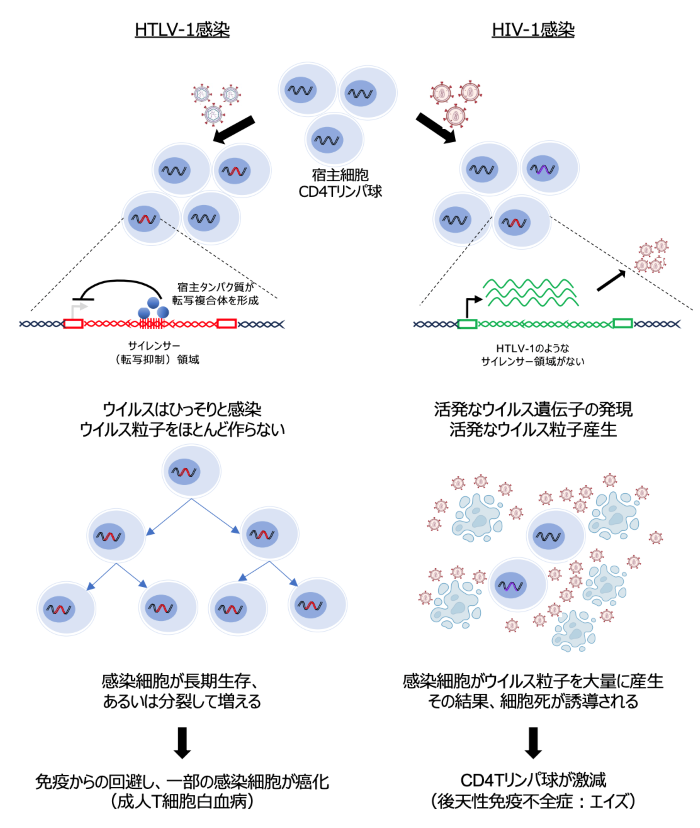
HTLV-1(ヒトT細胞白血病ウイルス1型)は主にCD4陽性T細胞に感染し、宿主ゲノムに組み込まれたプロウイルスとして長期に持続感染します。長い潜伏期間を経たのち、感染者の一部に成人T細胞白血病(ATL)などの疾患を発症します。Taxなど免疫原性の高いウイルス産物を持つにもかかわらず、多くの感染者ではウイルスは「低発現・低産生」へ傾き、免疫監視を回避して感染細胞クローンが維持されます。この「自発的な潜伏化」を規定する分子機構は、ウイルス発見以来の重要課題でした。
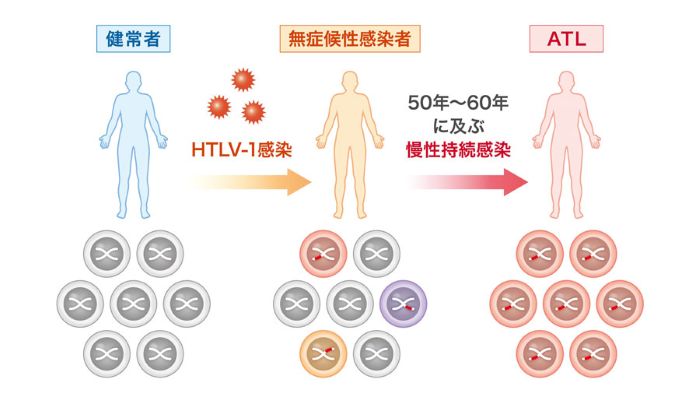
研究概要
本研究では、感染者検体を用いたクロマチン解析により、HTLV-1プロウイルス内部(pol領域に重なる位置)に「開いたクロマチン領域(OCR)」を同定しました。機能解析の結果、このOCRは5’LTR由来のセンス転写を抑制するシス制御配列として働き、HTLV-1の潜伏維持に寄与する「プロウイルス内サイレンサー」であることが示されました。
さらに、宿主転写因子RUNX1を中心とする複合体がこのサイレンサーに結合してウイルス発現を抑制すること、そしてサイレンサーが破綻するとHTLV-1の転写活性と免疫原性が増大することを明らかにしました。
主な成果
1.「ウイルス内サイレンサー」の同定
HTLV-1プロウイルス内部に新規OCRを見出し、転写抑制性のシス制御配列として機能することを示しました。
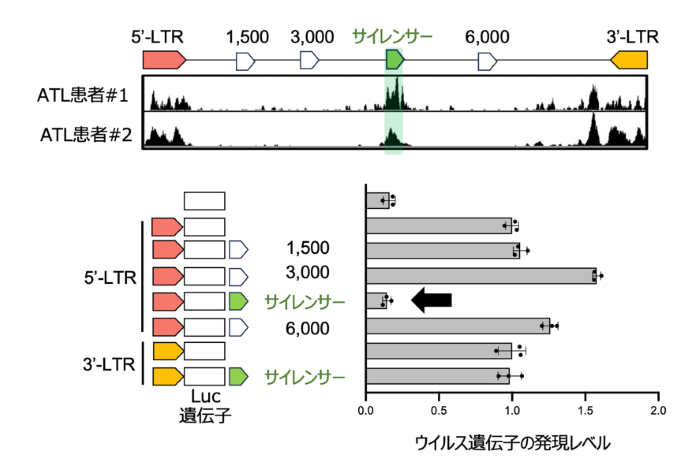
2.RUNX複合体による転写抑制機構
RUNX1を中心とする複合体がサイレンサーに結合し、HTLV-1の転写(転写バースト)を抑制する分子機構を提示しました。
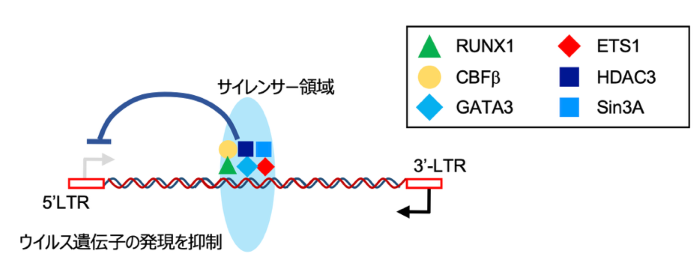
3.サイレンサー破綻がもたらす表現型
サイレンサーに変異が生じるとHTLV-1の複製と免疫原性が増大し、潜伏維持が「能動的制御」によって成立していることを支持する結果が得られました。
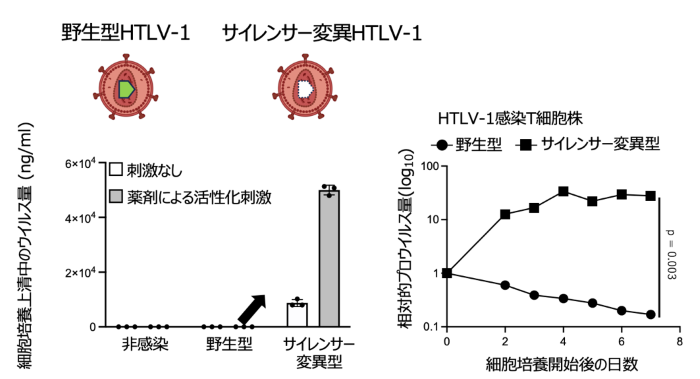
4.“潜伏モジュール”の可搬性(HIV-1への移植)
HTLV-1サイレンサーをHIV-1へ導入すると、HIV-1のウイルス産生が抑制されることを示しました。本結果は、レトロウイルス間での感染動態の差異を説明し得る新しい視点を提供します。
意義・今後の展望
本成果は、HTLV-1が免疫監視を回避しながら長期持続感染を成立させるために、自らのゲノム内に転写を抑制するサイレンサー領域を備えるという戦略を示しました。
サイレンサー-RUNX軸は、(1)潜伏解除による感染細胞の可視化と免疫排除、(2)再活性化抑制による病態惹起の抑制、という両方向の治療概念に接続し得る標的として位置づけられます。
論文情報・関連情報
- 掲載誌:Nature Microbiology
- 論文名:Intragenic viral silencer element regulates HTLV-1 latency via RUNX complex recruitment
- 著者:Kenji Sugata, Akhinur Rahman, Koki Niimura, Kazuaki Monde, Takaharu Ueno, Samiul Alam Rajib, Mitsuyoshi Takatori, Wajihah Sakhor, Md Belal Hossain, Sharmin Nahar Sithi, M. Ishrat Jahan, Kouki Matsuda, Mitsuharu Ueda, Yoshihisa Yamano, Terumasa Ikeda, Takamasa Ueno, Kiyoto Tsuchiya, Yuetsu Tanaka, Masahito Tokunaga, Kenji Maeda, Atae Utsunomiya, Kazu Okuma, Masahiro Ono & Yorifumi Satou
- 掲載日:2025年5月13日
- DOI:1038/s41564-025-02006-
